Un problème mondial en forte progression
Thank you for reading this post, don't forget to subscribe!La stéatose hépatique (communément appelée « foie gras ») est aujourd’hui l’une des maladies du foie qui croît le plus vite dans le monde. Elle englobe un large spectre : de la simple accumulation de graisses (stéatose) à la forme inflammatoire plus grave (stéato-hépatite, NASH) qui peut évoluer vers la fibrose, la cirrhose et le cancer du foie. Les estimations récentes montrent que la prévalence globale de la stéatose non alcoolique (NAFLD/MASLD) touche une part importante de la population adulte, avec des chiffres proches de 30–38% selon les méta-analyses et revues épidémiologiques les plus récentes. PubMed+1
Ce constat est inquiétant parce que la stéatose est souvent silencieuse : beaucoup de personnes ne savent pas qu’elles sont atteintes jusqu’à l’apparition de complications sévères. Des études récentes appellent à mieux dépister les populations à risque et à intensifier la prévention (alimentation, activité physique, contrôle du poids, diabète). The Guardian
Cet article donne des informations générales. Si vous pensez être concerné(e), consultez un médecin pour un diagnostic et un plan adapté (examens, bilan biologique et imagerie).
I. Qu’est-ce que la stéatose hépatique ?
La stéatose hépatique, souvent appelée foie gras, correspond à une accumulation excessive de graisses (surtout des triglycérides) dans les cellules du foie. Lorsque cette infiltration dépasse 5 % du poids du foie, on parle de stéatose.
Il existe deux grands types :
La stéatose non alcoolique, la plus fréquente, liée au surpoids, au sucre, à la sédentarité, à la résistance à l’insuline et parfois à certains médicaments. Elle n’est pas due à l’alcool.
La stéatose alcoolique, elle, résulte d’une consommation régulière ou excessive d’alcool, même modérée chez certaines personnes sensibles.
Les deux formes peuvent évoluer vers une inflammation plus grave du foie , puis vers la fibrose (durcissement d’un tissu dû à une accumulation de fibres) et la cirrhose( maladie du foie entraînant cicatrices, durcissement et mauvais fonctionnement) si les facteurs déclencheurs persistent.
La bonne nouvelle : la stéatose est réversible, surtout si elle est détectée tôt et corrigée par une meilleure alimentation, une perte de poids progressive et une activité physique régulière. journals.lww.com+1
Comparaison : foie sain, foie avec stéatose, accumulation de graisses intracellulaires.
II.Les 7 causes principales de la stéatose hépatique
Remarque : la stéatose est souvent multifactorielle, plusieurs causes peuvent coexister chez une même personne.
1. Surpoids et obésité abdominale (cause principale)
Le surpoids, et surtout l’obésité abdominale, constitue la première cause de stéatose hépatique. La graisse viscérale celle qui entoure les organes libère des hormones et des substances inflammatoires qui perturbent le métabolisme.
Elle favorise l’insulino-résistance(résistance à l’insuline qui assure le transport du sucre dans le sang), un état où les cellules répondent moins bien à l’insuline. Résultat : l’organisme dégrade davantage ses graisses (lipolyse), libère plus d’acides gras libres, qui se dirigent ensuite vers le foie.
Ce surplus surcharge le foie, provoque une accumulation de triglycérides et entretient une inflammation locale.
La bonne nouvelle : une perte de poids de seulement 5 à 10 % suffit souvent à réduire la graisse hépatique et à améliorer significativement la fonction du foie. . journal-of-hepatology.eu

Graisse viscérale : moteur métabolique de la stéatose hépatique.
2. Diabète de type 2 et résistance à l’insuline
Le diabète de type 2 s’accompagne presque toujours d’une résistance à l’insuline, ce qui perturbe la manière dont le corps utilise le glucose et les graisses.
Lorsque les cellules ne répondent plus correctement à l’insuline, l’organisme compense en produisant plus d’insuline, favorisant alors le stockage de graisses dans le foie.
Ce mécanisme augmente l’accumulation de triglycérides dans les cellules hépatiques et entretient une inflammation chronique du foie.
Ainsi, les personnes diabétiques sont beaucoup plus exposées au risque de stéatose non alcoolique, une forme inflammatoire de stéatose.
Elles présentent également une probabilité plus élevée d’évolution vers la fibrose et, à long terme, des complications hépatiques plus sévères. PubMed
3. Dyslipidémie (triglycérides élevés, cholestérol)
La dyslipidémie correspond à un déséquilibre des graisses dans le sang, notamment des triglycérides élevés et parfois du mauvais cholestérol (LDL).
Lorsque ces lipides circulent en excès, une partie est redirigée vers le foie, ce qui augmente l’accumulation d’acides gras dans les cellules hépatiques.
Cet afflux favorise progressivement la stéatose, puis l’inflammation du foie.
Une dyslipidémie non contrôlée augmente donc le risque d’évolution vers des formes plus sévères.
À l’inverse, corriger les lipides sanguins (alimentation, activité physique, médicaments si nécessaire) diminue considérablement cette surcharge.
La prise en charge globale permet ainsi de protéger le foie et de réduire les complications métaboliques.
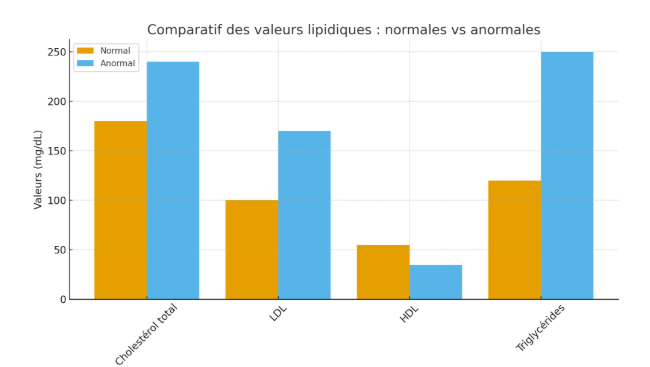
Graphe comparatif des valeurs lipidiques normales vs anormales: Dyslipidémie : facteur favorisant
4. Alimentation riche en sucres simples et graisses saturées
Les aliments ultra-transformés, boissons sucrées (sirops, sodas), excès de fructose et graisses industrielles augmentent le risque. Le foie transforme le fructose en lipides, contribuant à la stéatose.
Les types d’aliments à surveiller :
–Boissons sucrées : sodas, sirops, jus industriels riches en fructose.
–Pâtisseries et viennoiseries industrielles : riches en sucres rapides et graisses hydrogénées.
–Fast-foods : burgers, frites, nuggets, très riches en graisses saturées et trans.
–Céréales et snacks ultra-transformés : chips, biscuits, barres sucrées, gâteaux emballés.
–Produits sucrés à base de fructose concentré : bonbons, confiseries, sirop de maïs HFCS.

Aliments riches en sucres et graisses transformées : contributeurs majeurs.
5. Sédentarité
Un mode de vie inactif réduit la captation des lipides par les muscles et favorise l’accumulation hépatique. L’activité physique régulière améliore l’oxydation des graisses et réduit la stéatose, même sans perte de poids massive.

30 minutes d’activité modérée par jour réduisent le risque métabolique.
6. Médicaments et toxines
Certains médicaments (corticostéroïdes, méthotrexate, tamoxifène, etc.) et toxines peuvent provoquer ou aggraver la stéatose. Il faut toujours discuter des risques médicamenteux avec son médecin et son Pharmacien.

Certains traitements médicamenteux peuvent favoriser l’accumulation de graisses au foie.
7. Facteurs génétiques et ethnogénétiques
Des variants génétiques (ex. PNPLA3, TM6SF2) augmentent la susceptibilité individuelle. La distribution géographique et ethnique des gènes explique partiellement les différences de prévalence entre populations. pmc.ncbi.nlm.nih.gov
III.Signes cliniques et dépistage : comment savoir si on est concerné ?
La stéatose est souvent asymptomatique au début. Certains signes non spécifiques peuvent toutefois alerter : fatigue chronique, gêne ou douleur sourde au niveau de l’hypochondre droit, prise de poids difficile, ou altérations biologiques (élévation modérée des transaminases AST/ALT).
Examens courants
- Bilan biologique : transaminases (AST/ALT), bilan lipidique, glycémie à jeun, HbA1c.
- Imagerie : échographie abdominale (critère d’orientation), FibroScan (élastographie) pour estimer la fibrose.
- Autres : examens complémentaires selon suspicion (IRM hépatique, biopsie si doute sur la sévérité).
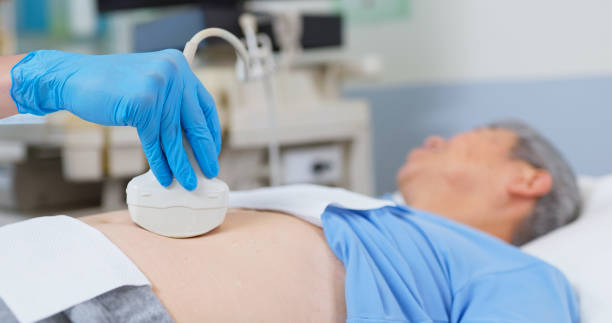
Echographie pour évaluer la stéatose et la fibrose.
4) Les risques si la stéatose n’est pas prise en charge
Sans prise en charge, la stéatose hépatique non alcoolique. peut évoluer vers la forme inflammatoire, puis vers la fibrose, la cirrhose, et dans certains cas le carcinome hépatocellulaire. En outre, la stéatose augmente le risque cardiovasculaire, les patients atteints de ont une mortalité cardiovasculaire plus élevée que la population générale. journals.lww.com+1
5) Le régime idéal pour « détoxifier » et protéger le foie : principes et exemple concret
Important : le terme « détoxifier » est populaire, dans un cadre médical, il s’agit surtout de réduire la charge lipidique hépatique, l’inflammation et l’insulino-résistance par l’alimentation et le mode de vie.
Principes nutritifs fondamentaux
- Réduction des sucres ajoutés et du fructose industriel (limiter sodas, jus sucrés, confiseries).
- Réduction des graisses trans et limitation des graisses saturées, privilégier les graisses insaturées (poissons gras, huiles végétales non raffinées).
- Apport en fibres (fruits, légumes, légumineuses, céréales complètes) pour améliorer la sensibilité insulinique.
- Protéines maigres (poisson, volaille, légumineuses) pour maintien de la masse maigre pendant perte de poids.
- Contrôle des portions et déficit calorique modéré si surpoids (objectif perte 5–10% du poids).
- Aliments anti-inflammatoires : fruits rouges, légumes verts, thé vert, oméga-3.
- Hydratation suffisante et limitation de l’alcool (en NAFLD, l’alcool doit être restreint).
Exemple de plan alimentaire journalier (modèle)
- Petit-déjeuner : yaourt nature ou fromage blanc + flocons d’avoine + fruits rouges + graines (chia/graines de lin).
- Collation (si besoin) : une pomme ou une poignée d’amandes.
- Déjeuner : salade variée (légumes crus + quinoa) + filet de saumon grillé + huile d’olive + légumes cuits.
- Goûter : yaourt végétal ou une orange.
- Dîner : poulet grillé + légumes rôtis + patate douce en petite portion.
- Hydratation : eau, tisanes, thé vert (modération). Éviter les sodas, limiter les jus de fruits.

Aliments anti-inflammatoires pour un foie sain
Aliments à privilégier :
- Poissons riches en oméga-3 (saumon, maquereau).
- Légumes crucifères (brocoli, chou) , propriétés protectrices.
- Fruits rouges (antioxydants).
- Avoine, légumineuses (fibres).
- Huile d’olive extra vierge (graisses mono-insaturées).
- Thé vert (catéchines).
Aliments à limiter ou éviter
- Boissons sucrées, jus industriels, friandises.
- Fritures, aliments ultra-transformés.
- Excessive consommation d’alcool.
- Excès de viandes grasses et charcuteries.
6) Compléments alimentaires : lesquels ont des preuves et quelles sont leurs limites ?
Toujours en parler avec son médecin/pharmacien — les compléments aident parfois mais ne remplacent pas l’alimentation et l’activité.
1. Oméga-3 (EPA/DHA)
Des études montrent une réduction des triglycérides et parfois une amélioration de la stéatose à l’imagerie. Les doses thérapeutiques sont généralement plus élevées que l’apport alimentaire habituel (ex. 2–4 g/j d’EPA+DHA selon étude). Preuve modérée.
2. Vitamine E (α-tocophérol)
Dans certaines études chez des patients non-diabétiques atteints de NASH, la vitamine E a montré une amélioration histologique. Son usage doit être prudent (dose et durée médicalement supervisées).
3. Silymarine (extrait de chardon-marie)
Usage traditionnel et études petites à modérées suggèrent un effet hépatoprotecteur ; données cliniques encore hétérogènes.
4. Probiotiques / prébiotiques
La modulation du microbiote intestinal peut influencer le métabolisme hépatique. Certaines souches montrent un bénéfice modeste sur les enzymes hépatiques et la stéatose, mais la recherche est encore active.
5. Thé vert (extraits de catéchines)
Le thé vert et ses catéchines sont associés à des effets antioxydants et métaboliques bénéfiques ; les extraits peuvent aider mais attention aux doses élevées (hépatotoxicité rare avec extraits très concentrés).
Les compléments peuvent être utiles en accompagnement (notamment oméga-3, vitamine E chez certains profils, la silymarine), mais la preuve n’est pas universelle et l’accompagnement médical est essentiel. Les changements d’habitudes restent la pierre angulaire du traitement.
7) Conseils pratiques et plan d’action en 8 semaines (programme simple à suivre)
Objectifs principaux
- Perte de 5–10% du poids si surpoids.
- Réduction des sucres ajoutés et aliments ultra-transformés.
- 150–200 minutes d’activité modérée par semaine + renforcement musculaire 2×/semaine.
Semaine 1–2 : Diagnostic et préparation
- Faire un bilan médical (transaminases, glycémie, lipides).
- Remplacer boissons sucrées par eau/infusions, commencer marche 20–30 min/jour.
Semaine 3–4 : Changement alimentaire progressif
- Introduire 2 portions de légumes verts/ jour, 3 portions de fruits rouges/semaine.
- Remplacer fritures par cuisson au four/poêle avec peu d’huile.
Semaine 5–6 : Intensification de l’activité
- Monter à 30–45 min d’activité modérée 5×/semaine; ajouter 2 séances de renforcement (sangles, poids légers).
Semaine 7–8 : Stabilisation et suivi
- Réévaluer poids et objectifs; contrôles biologiques si prescrits.
- Envisager complément (oméga-3) si le médecin le recommande.
Conclusion
Messages clés à retenir
- La stéatose hépatique est très fréquente et souvent silencieuse ; la prévention et le dépistage ciblé sont essentiels. journals.lww.com+1
- Les facteurs principaux sont le surpoids, la résistance à l’insuline, l’alimentation riche en sucres simples et la sédentarité, la plupart sont modifiables par le mode de vie.
- Le « régime idéal » pour réduire la stéatose combine décalage calorique modéré (si surpoids), réduction des sucres ajoutés, lipides de qualité (oméga-3, huile d’olive), fibres et activité physique régulière.
- Certains compléments (oméga-3, vitamine E, silymarine) peuvent aider, mais doivent être prescrits ou validés par un professionnel de santé.
- Si vous êtes concerné(e) : faites un bilan médical, suivez un plan d’action progressif et priorisez les changements d’habitudes durables.
👉👉Complément alimentaire disponible sur Amazon: Ortis DépurFoie 60 comprimés